科研进展
2015:心血管重塑相关疾病研究阶段性进展——心血管重塑相关疾病病理生理学机制研究进展
炎症微环境在高血压致纤维化中起重要作用。杜杰课题组针对高血压条件下炎症微环境是启动、形成的、炎症细胞间相互作用进而参与纤维化进行系列研究,发现:
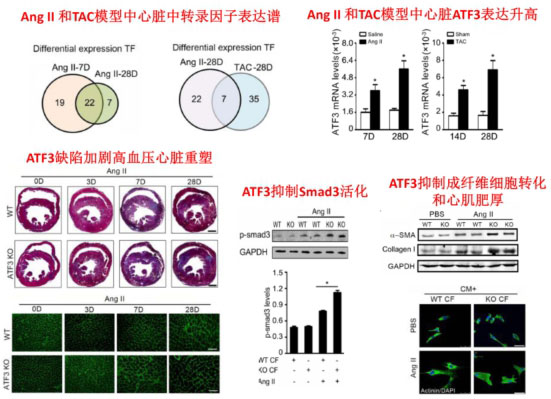
(1) 转录因子ATF3发挥抗高血压性病理性重塑的保护作用
利用AngII灌注和压力后负荷2种高血压疾病模型,通过转录组学测序,发现高血压激活心脏中转录因子ATF3表达。ATF3缺失加剧高血压性心脏纤维化和心肌肥厚。通过chip-seq首次发现,ATF3抑制TGF-beta/smad-3通路,抑制成纤维细胞分化,进而通过旁分泌作用抑制心肌肥厚。
(2) 内源性α7-尼古丁乙酰胆碱受体抗炎通路抑制高血压性心力衰竭
课题组的研究发现AngII灌注介导心脏中α7-尼古丁乙酰胆碱受体(α7nAchR)升高,通过骨髓移植实验明确骨髓源性a7nAchR缺失加剧心力衰竭。机制上,a7nAchR活化单核细胞释放IL-1β、TNF-α等促炎因子,促进单细胞-内皮粘附,加剧心脏中炎症反应,最终导致心脏损伤和病理性重塑。

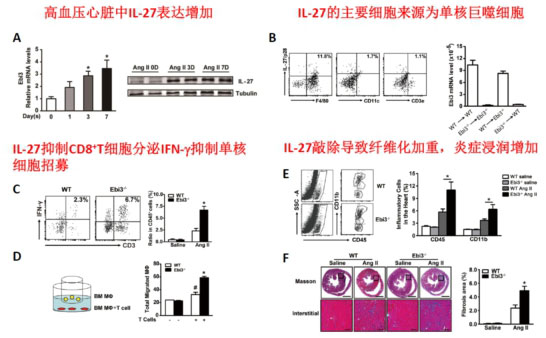
(3)IL-27抑制高血压心脏损伤
课题组研究发现高血压小鼠的心脏组织中IL-27的mRNA和蛋白的水平增加,骨髓移植实验显示IL-27的主要细胞来源是单核巨噬细胞。IL-27 Ebi3亚基敲除导致Ang II灌注的心脏组织中炎症浸润增加,心脏纤维化加重。敲除小鼠进一步祛除CD8阳性T细胞可以减轻炎症反应和纤维化,而CD4阳性T细胞祛除无影响。 体外细胞共培养显示IL-27通过抑制CD8+T细胞分泌IFN从而抑制趋化因子的表达,减少单核巨噬细胞的招募。
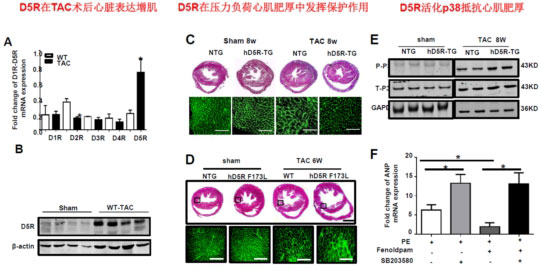
(4)多巴胺D5受体活化抑制压力负荷导致的心肌肥厚
课题组研究发现TAC术后心脏中D5R表达增加,使用D5R全身过表达小鼠和D5R基因功能缺失小鼠,证实了D5R在压力负荷所致心肌肥厚中具有保护。机制方面,发现多巴胺受体5通过激活P38发挥心肌保护作用。
(5)高性能阳离子基因载体介导mir-29b导入抑制心脏纤维化
课题组研究发现EA功能化的聚甲基丙烯酸缩水甘油酯(PGEA)材料具有较低的细胞毒性。利用BIBB修饰的季戊四醇(PER)作为引发剂,进行ATRP聚合,并通过后续的EA功能化,合成以PER为核心的星型聚合物基因载体PER-PGEA阳离子材料,增强其基因传递效率。利用PER-PGEA为载体络合mir-29,有效将mir-29导入心脏,抑制mir-29下游细胞外基质蛋白表达降低,发挥抑制心脏纤维化的作用。

冠心病是全球死亡率最高的疾病之一,近年来在我国的发病率逐年升高,随着介入治疗的广泛开展和冠状动脉旁路移植手术的实施,有效地解决了多种复杂和危重类型冠心病,但之后病变部位血管再狭窄的发生成为困扰临床的又一问题。我们的研究以炎症反应为核心,以静脉-动脉移植及导丝拉伤造成血管损伤为基础,进行了系列的研究,主要阐明了: 1)血管损伤及新生内膜重塑是一个T淋巴细胞、血小板细胞、巨噬细胞、内皮细胞、平滑肌细胞、成纤维细胞等参与的炎症反应过程;2)T淋巴细胞、血小板细胞、巨噬细胞对于血管管壁细胞的增殖分化及细胞外基质的生成与降解的作用。我们的研究为血管损伤后重塑,尤其是新生内膜形成的机制和治疗提供理论和实验基础。
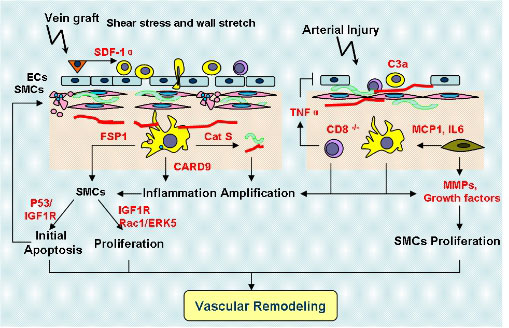
我们的另一个研究方向为大血管病变主动脉瘤的发病机制。主动脉瘤因其起病隐匿,易发生瘤体破裂,具有极高的死亡率。我们的研究集中于炎症在在血管外基质降解及主动脉瘤发生中的作用。
主要进展如下:
(1)利用小鼠下腔静脉移植到颈总动脉建立静脉-动脉移植模型,研究移植静脉血管重塑的机制。
(A)首次发现CARD9介导了坏死平滑肌的促炎性作用,促进了移植静脉新生内膜增厚
在静脉移植中,由于移植的静脉血管暴露于动脉血循环中,主要受到机械张力的作用,诱导平滑肌细胞的早期凋亡和后期增殖,从而引起移植静脉的狭窄和闭塞。CARD9在巨噬细胞和树突状细胞中介导固有免疫。我们发现在移植静脉的巨噬细胞中存在CARD9的高表达,并且移植静脉中存在平滑肌细胞坏死,坏死的平滑肌细胞可以激活巨噬细胞中NF-κB通路,从而介导炎症因子的表达,CARD9敲除后可以抑制NF-κB的激活,抑制平滑肌细胞的迁移,抑制移植静脉新生内膜的形成。(Cardiovasc Res. 2015;108(1):148-58.)

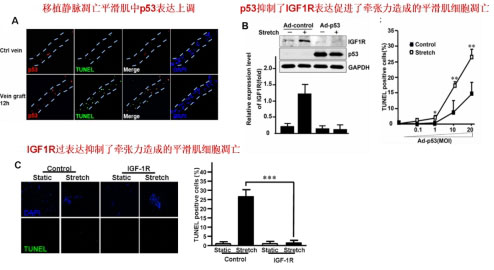
(B) 发现p53/IGF1R信号介导了移植静脉平滑肌细胞早期凋亡
静脉移植入动脉后由于血流及血管牵张力的改变会发生以早期平滑肌细胞凋亡为特征的血管重塑,这对静脉血管的动脉化及移植术的预后至关重要。我们发现在静脉移植术后12小时,植入静脉血管的平滑肌细胞即发生凋亡,检测到凋亡平滑肌细胞中p53蛋白表达升高,随后p53介导了机械牵张诱导的静脉平滑肌细胞凋亡。在植入静脉血管中p53与IGF-1R的表达水平呈负相关,在平滑肌细胞中过表达p53可以降低牵张所诱导的IGF-1R表达。我们发现在植入静脉的凋亡平滑肌细胞中IGF-1R的表达水平降低,而增加IGF-1R的表达则可以抑制机械牵张所造成的平滑肌细胞凋亡,因而IGF-1R的下调是移植静脉中机械牵张造成平滑肌细胞凋亡的可能机制。
(2) 利用小鼠股动脉导丝损伤模型,研究动脉损伤后新生内膜形成的机制。
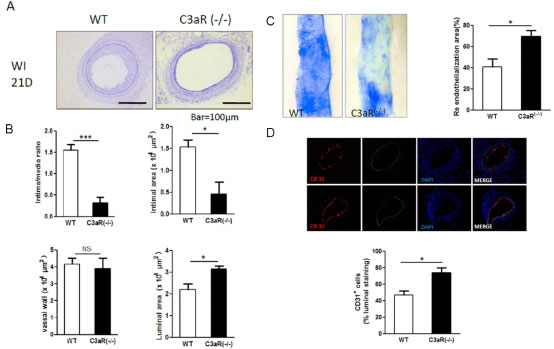
C3a受体敲除抑制了动脉损伤后新生内膜形成
在导丝损伤的股动脉血管中,补体C3a受体(C3aR)的表达升高,主要定位于巨噬细胞细胞。敲除C3aR抑制了动脉损伤后新生内膜的形成。进而发现C3a敲除改善了损伤血管的再内皮化。在体C3aR敲除后明显降低了血浆中IL-6的水平,同样巨噬细胞中C3aR敲除也明显减少了C3a刺激的IL-6表达。而IL-6敲除小鼠与野生型相比减轻了新生内膜增厚,提示C3a通过IL-6促进了动脉损伤后新生内膜形成。(Cardiovasc Res修稿)
(3)利用BAPN诱导的小鼠主动脉夹层模型,研究主动脉瘤及夹层发生的病理机制并确定致病位点。
(A)我们在小鼠中利用LOX抑制剂BAPN饲喂建立了主动脉夹层模型,检测了此模型的基本特征,并比较了不同种属的小鼠诱导此模型的区别,为以后主动脉瘤/夹层病因及病理机制研究提供了基础,文章已投稿至Journal of Vascular Surgery。
(B)内质网应激造成血管平滑肌细胞凋亡促进主动脉夹层形成
主动脉夹层是发病凶险,死亡率极高的大血管疾病。在主动脉夹层的病理过程中存在平滑肌细胞的大量死亡,进一步导致血管壁薄弱,促进夹层的形成。我们利用lysyl oxidase抑制剂BAPN饲喂小鼠,建立主动脉夹层的模型,发现夹层平滑肌细胞内质网应激(ER stress)被活化(CHOP,ATF4高表达),探寻ER stress活化原因,我们发现BAPN抑制了弹力蛋白与胶原蛋白的交联,从而使主动脉壁变薄弱,平滑肌细胞受到的牵张力增强,高牵张力可以激活ER stress,并介导炎症。CHOP-/-可以抑制ER stress介导的炎症和平滑肌细胞凋亡,从而减少主动脉夹层的发生。(J Pathol. 2015;236(3):373-83.)

(C)C3a-C3aR信号促进主动脉夹层的发生与破裂
在主动脉夹层模型和病人样本中可以观察到补体系统活化。而抑制补体C3aR或敲除C3aR可以抑制主动脉夹层的发生和破裂,文章准备投稿。
(D)主动脉夹层可疑致病位点基因工程小鼠建立
基于实验室前期测序获得的主动脉夹层可疑致病位点,我们利用CRISPR/Cas9技术建立了基因工程小鼠平台,已成功建立转基因小鼠3个品系,基因敲除小鼠3个品系,点突变小鼠3个品系,另有十余个品系的点突变小鼠在建立过程中,为后续致病位点确定和病理机制研究提供基础。
针对高血压、急性心肌梗死介导的心脏损伤、病理性重塑和心衰的发病机制展开研究,以心脏炎症微环境的建立为核心,利用多种组学技术,发现了一些新的介导心脏损伤的靶分子,深入探讨多种炎性细胞、炎症介质、心脏实质细胞的相互作用介导心脏损伤/病理性重塑的机制,结合新的阳离子载体材料开展抗心脏纤维化的治疗工作。
杜杰团队相关工作进展如下:
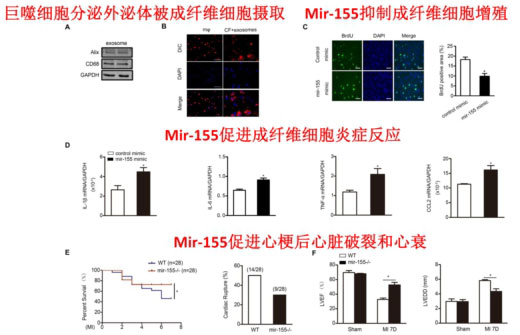
(1)巨噬细胞分泌mir-155促进急性心梗不良修复
巨噬细胞分泌含mir-155的外泌体被成纤维细胞摄取;exosome中的mir-155可以通过抑制Sosc1进而抑制成纤维细胞的增殖及抑制Sosc1促进成纤维细胞的炎症反应;利用结扎冠状动脉前降支模拟急性心肌梗死模型,抑制mir-155的表达后可通过促进心脏成纤维细胞的增殖以及抑制心脏的炎症反应进而改善急性心肌梗死后的心功能。
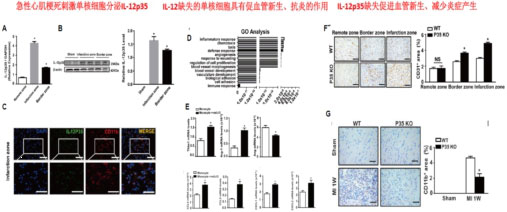
(2)IL-12抑制心梗后心脏修复
课题组的研究急性心肌梗死刺激单核细胞产生IL-12增加,通过IL-12基因缺失小鼠和IL-12中和抗体均以改善心梗后心脏功能和修复;分离梗死心脏中单核细胞,进行转录组测序发现IL-12缺失导致单核细胞向促血管新生、抑炎的方向分化,从而抑制心脏损伤,促进心梗后心脏修复。(工作发表在Cardiovascular Research.2015)。
(3)C3aR抑制急性心梗后心脏破裂
课题组的研究发现心肌梗死后心脏中有活化补体C3b沉积,补体C3a受体缺失小鼠心梗后死亡率增加,心脏破裂增加,心功能降低。C3aR-/-小鼠在心梗早期心脏中心肌细胞凋亡增加,炎症细胞浸润增加。骨髓交叉移植的结果显示心脏原位的C3aR缺失会导致心梗后心脏破裂和死亡率的增加。体外实验显示C3a可以通过激活C3aR下游的AKT信号通路,增加Foxo1的出核和降解,从而抑制缺氧时心肌细胞的凋亡。特异性敲除心肌细胞中的Foxo1可以明显减少心梗后心肌细胞的凋亡和小鼠死亡率。
李汇华教授团队主要研究成果如下:
(1)MicroRNA Let-7i负性调节心肌纤维化:
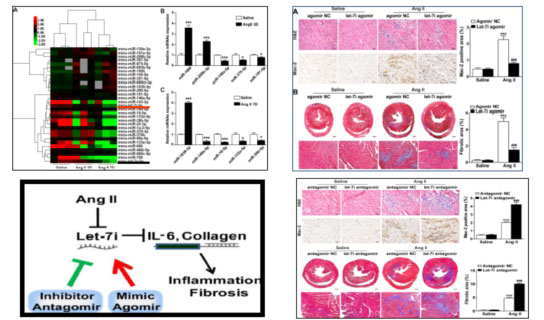
(2)蛋白酶体激活通过下调ATRAP促进血管紧张素II诱导的心肌肥大:
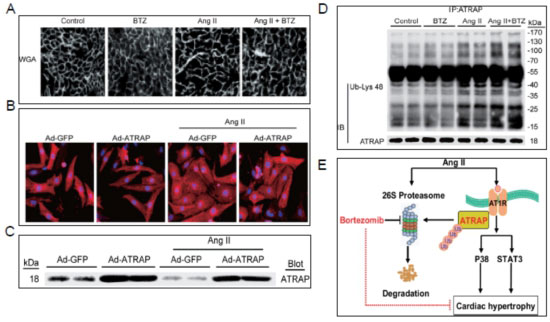
(3)急性心梗患者血清中一新的敏感性标记物:E3连接酶RNF207:

刘慧荣课题组研究方向:自身免疫与代谢性心血管疾病易感性研究,工作进展如下:
(1)衰老研究工作进展:
证实了心肌组织中促凋亡蛋白Omi/HtrA2在衰老过程中mRNA水平增加的上游调控机制以及线粒体中增加的Omi/HtrA2促caspase途径活化的机制。主要发现如下:1.老龄(24月龄)小鼠心脏储备能力下降,例如,在增加运动负荷后衰老小鼠心功能明显下降;2. 小鼠心肌组织中Omi/HtrA2的mRNA水平与心脏收缩功能成负相关;3. 明确了Omi/HtrA2基因启动子的核心区域;4. 证实了衰老心肌细胞线粒体中增加的Omi/HtrA2可以促进细胞色素C的释放从而激活caspase依赖的线粒体凋亡途径。
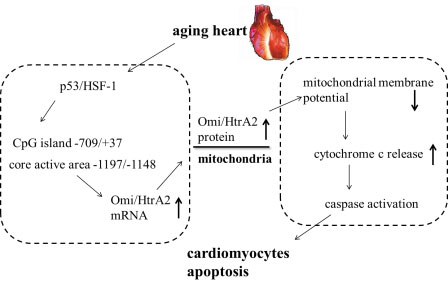
(2)β1-AA研究工作进展:
β1-AA可促进健康BALB/c小鼠调节性T淋巴细胞(Treg cells)活化,同时β1-AA可在离体水平直接通过β1AR途径诱导天然调节性T淋巴细胞(nTreg cells)分化;较高浓度的 β1-AA可抑制nTreg cells活化,并削减nTregs cells对心肌细胞的保护作用;2. β1-AA可在离体水平促进成纤维细胞增殖,经β1AA作用后的成纤维细胞上清可损伤乳鼠心肌细胞;3. β1-AA可通过活化T淋巴细胞促进健康BALB/c小鼠胰岛损伤、血糖升高;β1-AA可通过β1AR途径导致NIT-1胰岛细胞系损伤并抑制其胰岛素的分泌。
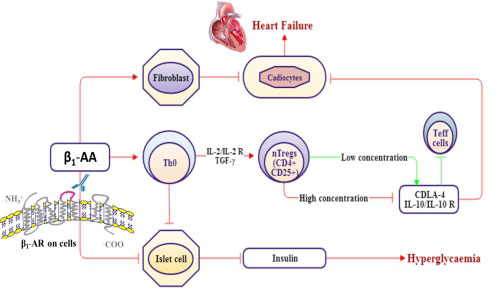
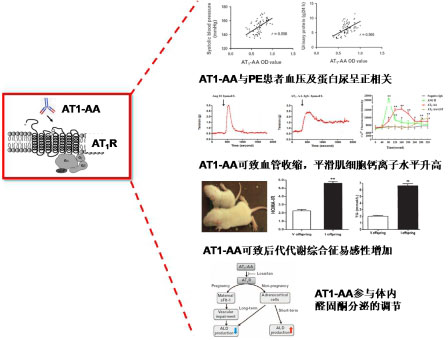
(3)AT1-AA研究工作进展:
血管紧张素Ⅱ1型受体自身抗体(AT1-AA)首先在子痫前期患者血清中发现,进一步研究证实其可以激活血管紧张素Ⅱ1型受体而发挥类似血管紧张素Ⅱ的作用。本研究室的研究发现:(1)AT1-AA与子痫前期病人的血压及蛋白尿水平呈正相关,在重度子痫前期的患者血清中AT1-AA的阳性率为100%。(2)AT1-AA可收缩胸主动脉、冠状动脉、大脑中动脉、胎盘动脉以及肠系膜动脉。在细胞实验中观察到AT1-AA引起血管平滑肌细胞内钙离子浓度长时间升高,可能与其收缩血管的机制相关。而且,AT1-AA还可引起内皮细胞的损伤。(3)妊娠大鼠,AT1-AA不仅对母体造成损伤,还可对后代的健康造成影响。我们发现AT1-AA阳性孕鼠的后代体重离散度大,对代谢综合征易感性增加。(4)AT1-AA的存在对体内醛固酮水平产生影响,利用H295R细胞发现,短期低浓度的AT1-AA可促进细胞增殖,醛固酮分泌增加;长期高浓度的AT1-AA可导致细胞坏死和凋亡,醛固酮分泌减少。

 京公网安备 11010502031208号
京公网安备 11010502031208号