科研进展
2014:心血管重塑相关疾病的分子病因学研究——心肌病病因学研究
心肌病是一种原因不明的心肌疾病,它不包括病因明确的或继发于全身疾病的特异性心肌病。心肌病可分为三种:扩张型心肌病(DCM),肥厚型心肌病(HCM)和限制性心肌病(RCM)。其中以HCM和DCM较为常见。HCM患者常有严重症状,易发生房性、室性心率失常以及猝死。DCM临床表现为进行性心力衰竭(心衰)、左室收缩功能下降、室性及室上性心律失常、传导系统异常、血栓栓塞及猝死,并可发生在病程中任何阶段的疾病,对家庭和社会造成严重的负担,是心衰的第三大病因及心脏移植最常见原因。对HCM和DCM传统的诊断方法只能在心肌出现不可逆病理改变之后才能做出诊断,且不能预测猝死发生的危险性,因此若能在此前对预后做出判断,并对高危患者进行干预,意义十分重大,基因突变的研究使这成为可能。
心肌病的发病原因至今未明。DCM的分子遗传学研究成果有家族史的约占20%~35%,已报道的30多个DCM的致病基因主要是由心肌结构蛋白突变。50%的HCM患者有遗传倾向,散发病例逐年增多,现已报道的与该疾病有关的致病基因主要为10多个心脏肌小节基因,总计有几百个突变位点。但目前这些资料均来自国外,中国的HCM或DCM的遗传学基础目前还不清楚,有关中国人群的心肌病的基因分布及基因突变数据库目前尚未作系统研究。勾划我国心肌病的致病基因分布情况,探询基因型与表现型的关系,对病人进行早期的危险分层,早期预防,改善生存质量及延长患者的寿命意义重大。
课题组已开展心肌病致病基因的初步研究工作。已收集国人HCM样本150余例和DCM样本100余例,建立了中国汉族人群HCM和DCM遗传样本库平台,收集了患者的临床资料,包括体检、心电图、超声心动图检查。已经建立基因诊断的基因捕获测序试剂盒,并采用此技术,对收集到的心肌病样本的目标区域进行个体化捕获测序,对其目标序列进行生物信息学分析。目前已为多个肥厚型心肌病家系确定了个体化的致病基因,从基因水平进行了确诊,同时对已知致病基因在中国汉族HCM人群的分布情况进行了全面的估价。对于未找到致病突变的家系,课题组采用了全外显子捕获测序技术,去寻找国人心肌病的新的致病基因,并去了解新致病基因与国人心肌病发生发展的关系。
前期工作利用实验室设计的捕获试剂盒对117个肥厚型心肌病患者,进行了目标区域捕获测序。对22个已知致病基因进行数据分析后,共发现21个已知致病突变,同时,为多个肥厚型心肌病的家系作出了基因诊断。在未发现已知致病突变的样本中,经过数据库的过滤,位点致病性分析,最终发现28个新致病,这些新致病突变将进行遗传学和功能学的验证,明确这些致病突变的作用机制。
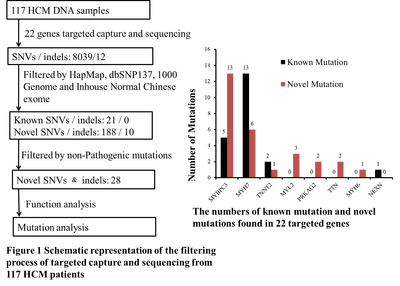
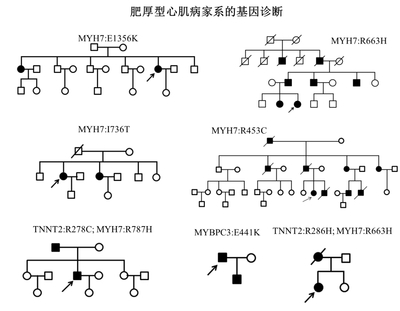
分子遗传学研究表明,大约70%的HCM病例是由编码肌节组成蛋白基因的突变引起的。但是这些肌节蛋白突变导致心肌肥大和心律失常的机制还不清楚。早期的HCM研究采用了生物化学和生理学方法,对HCM病人的骨骼肌细胞或转基因动物的心肌细胞进行了分析,结果提示这些突变降低了肌细胞的收缩能力并产生代偿性的肥厚。最近,几个重要的研究采用表达MYH6 R403Q突变的转基因小鼠,发现心肌细胞的收缩力增强并且伴随有更高的能量消耗,是HCM产生的主要原因1-2。由于没有理想的研究模型,这些相互矛盾的结果导致HCM的发生机理存在非常多的争议。产生这一问题的主要原因,是大多数已知的心血管疾病相关的分子信号通路,都是通过非人类过表达系统或者转人基因动物模型获取的,其中最主要的是转基因小鼠。然而,人鼠基因组之间存在着显着的差异,尤其是人类具有很多的独有的调控因子,因此小鼠模型有很大的局限性。另一个主要的问题是不同种属心肌细胞,乃至心脏之间的电生理学特性之间存在很大差异,很多人类特有的心脏生理异常无法在动物模型中研究。例如,静息状态下小鼠的心率是人的8倍以上,他们对运动和心率失常的生理反应也有很大差异。以HCM研究为例,人心室肌主要表达MYH7,而小鼠主要表达MYH6。由于人类HCM已知突变一半左右发生在MYH7,小鼠HCM模型对于此类突变并不适用。因此,我们需要一个人源的心肌细胞模型来研究HCM的发生机制。
兰峰教授研究主要基于在心血管疾病机制的研究,延续了所采用的经典心脏生理学分析技术,并增添了目前最新的细胞分化培养技术和高通量测序技术,大大加强了原有HCM研究的创新性。对于本研究中所采用的几个关键的新技术,进行了前期探索性实验,并且取得的较为理想的结果,汇报如下:
尿样细胞收集与重编程
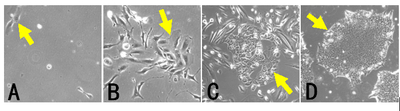
A.刚贴壁并开始分裂的尿样细胞B. 尿液上皮细胞形成的细胞群 C. 重编程过程中的尿液上皮细胞中出现的iPSCs样克隆 D. 挑取后培养扩增的iPSCs。
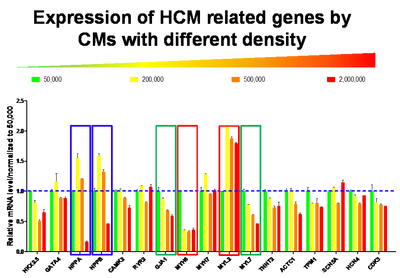
不同密度下iPSCs-CM基因表达的差异
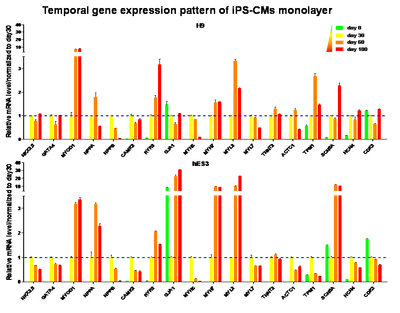
不同培养时间iPSCs-CM基因表达的差异,细胞年龄从未分化iPSCs的0天到180天。

 京公网安备 11010502031208号
京公网安备 11010502031208号